截止到2021年5月31日,最近全球肿瘤领域新药临床重大进展共计11项

导语:
根据公开资料不完全统计,截止到2021年5月31日,NextPharma为大家收录到了最近的全球肿瘤领域新药临床重大进展共计11项。现整理如下:
1.肺癌
基石药业PD-L1治疗III 期NSCLC注册性临床试验成功,拟递交新药上市申请
5月28日,基石药业宣布代号为GEMSTONE-301的注册性临床试验在计划的期中分析中达到了预设的主要研究终点。该研究旨在评估抗PD-L1单抗舒格利单抗作为巩固治疗在同步或序贯放化疗后未发生疾病进展的、局部晚期/不可切除(III期)非小细胞肺癌(NSCLC)患者的有效性和安全性。
试验结果显示,与安慰剂相比,舒格利单抗显著改善盲态独立中心评估(BICR)的无进展生存期(PFS),差异具有统计学显著性与临床意义。舒格利单抗的安全性良好,未发现新的安全性信号。亚组分析显示,无论同步还是序贯放化疗后的患者均显示出临床获益。
据悉,舒格利单抗是全球首个显著改善同步或序贯放化疗后无疾病进展的III期NSCLC患者PFS的PD-1或PD-L1单抗,同时也是全球首个同时覆盖局部晚期/不可切除(III期)和转移性(IV期)NSCLC全人群的PD-1或PD-L1单抗。
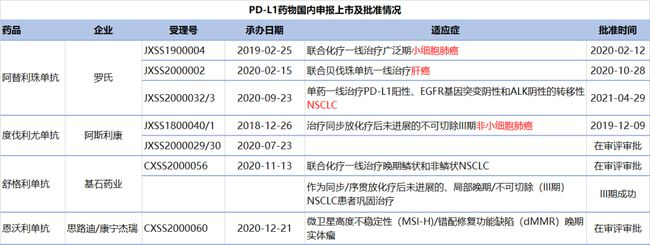
由PharmaGo数据库可知,目前国内已有2款PD-L1单抗获批上市,2款处于申报上市阶段。从下表可看出阿斯利康度伐利尤单抗获批适应症针对的III期NSCLC人群只是同步放化疗患者,而基石药业在GEMSTONE-301研究中还入组了序贯放化疗患者,覆盖人群更广。
2.乳腺癌
默沙东Keytruda早期三阴性乳腺癌新辅助/辅助III期研究达到EFS主要终点
5月14日,默沙东宣布代号为KEYNOTE-522的关键III期临床研究获得积极结果,达到了第2个主要终点无事件生存期(EFS)。根据独立数据监测委员会(DMC)的中期分析,与单纯术前化疗相比,Keytruda联合化疗作为新辅助治疗,术后继续单药作为辅助治疗可使高危早期三阴性乳腺癌(TNBC)患者的EFS具有统计学和临床意义的改善。Keytruda是首个在TNBC新辅助/辅助治疗中显示出EFS显著统计学意义的PD-1疗法。
该研究的另一个主要终点pCR(病理完全缓解)的分析数据已公布于2019年欧洲医学肿瘤学会(ESMO)大会上,并发表在《NEJM》。结果显示,Keytruda联合化疗新辅助序贯Keytruda辅助用于早期TNBC相比安慰剂+化疗新辅助序贯安慰剂辅助可使pCR显著改善(64.8% vs. 51.2%,P=0.00055),无论PD-L1状态如何。
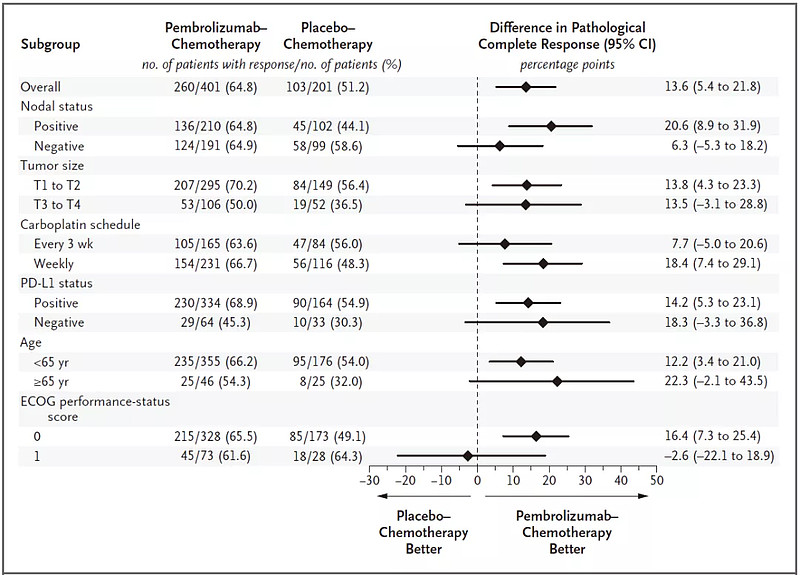
图:KEYNOTE-522研究中试验组与对照组病理学完全缓解(ypT0/Tis ypN0期)百分比差异的亚组分析(来源:NEJM)
3.新型免疫组合疗法
LAG-3/PD-1组合疗法(nivolumab+relatlimab)首个III期数据公布
5月19日,百时美施贵宝(BMS)公布了代号为RELATIVITY-047的II/III期临床试验数据,该试验结果表明,与Opdivo单药治疗相比,固定剂量抗LAG-3抗体relatlimab和抗PD-1抗体nivolumab(Opdivo)组合疗法一线治疗转移性或不可切除黑色素瘤,无进展生存期(PFS)具有显著统计学意义和临床获益。
研究结果显示,联合治疗组的中位PFS为10.12个月,显著长于Opdivo单药治疗组的4.63个月 ([HR] 0.75; 95% CI: 0.62-0.92, p=0.0055)。Nivolumab + relatlimab组合疗法的安全性可控,与之前报道的情况一致。3/4级药物相关不良事件(TRAE)发生率为18.9% vs 9.7%,因TRAE导致停药的患者比例为14.6% vs 6.7%。
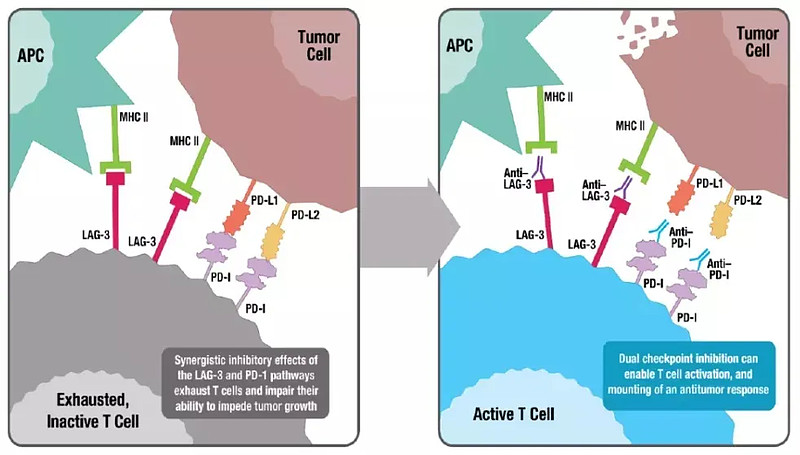
淋巴细胞激活基因-3(LAG-3)和程序性死亡受体-1(PD-1)是两种不同的抑制性免疫检查点,通常共同表达于肿瘤浸润淋巴细胞(TILs),并导致肿瘤介导的T细胞衰竭。
据悉,这是抗LAG-3抗体III期临床试验数据的首次展示,同时也是首个在转移性黑色素瘤中相比抗PD-1抗体单药治疗显示出统计学优势的治疗方案。详细数据将在2021年美国临床肿瘤学会(ASCO)年会期间的口头报告呈现。
值得一提的是,5月14日,LAG-3单抗Relatlimab和PD-1单抗Opdivo组成的固定剂量复方注射液临床申请获CDE受理。
4.度伐利尤单抗联合替西木单抗首个显示出OS获益的III期试验
5月7日,阿斯利康公布了POSEIDON研究最终数据。这项代号为POSEIDON的III期研究旨在探索度伐利尤单抗+铂类化疗、度伐利尤单抗+替西木单抗+化疗 vs 单独化疗在 IV 期(转移性)NSCLC患者一线治疗的疗效和安全性。
结果表明,与单独化疗相比,度伐利尤单抗、替西木单抗和化疗的组合显示出具有统计学意义和临床意义的总生存 (OS) 益处。该研究此前分析表明,度伐利尤单抗+化疗 vs 化疗显著改善了PFS,但OS未显示出显著的统计学差异。
5.早期临床进展里程碑
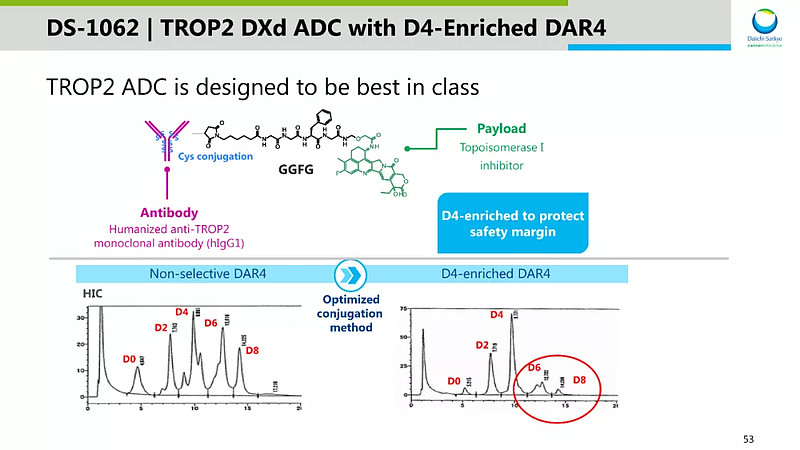
2021-05-08:第一三共与阿斯利康公布了datopotamab deruxtecan(DS-1062 )治疗转移性三阴性乳腺癌的1期试验TROPION-PanTumor01(NCT03401385)初步数据。
研究结果显示,在21例可评估患者中,ORR达到43%,5例达到确证的CR/PR。DCR为95%。未出现AEs相关的治疗暂停。6例患者因AEs剂量减少,主要是因为腔炎(13%)和粘膜炎症(8%)。33%患者观察到3级或以上TRAEs。
6.急性髓系白血病或高危骨髓增生异常综合征
2021-05-12:Curis公布IRAK4抑制剂CA-4948治疗急性髓系白血病或高危骨髓增生异常综合征的1/2期试验(NCT04278768)中期数据。在9例可评估患者中,8例在所有剂量中均观察到骨髓母细胞减少,1例患者观察到血液学完全缓解,1例CRi伴微小残留病灶阴性,2例骨髓CR。3例伴有SF3B1或U2AF1剪接体突变的患者达到骨髓CR或更佳。
7.骨髓增生异常综合征和急性髓系白血病
2021-05-19:Jasper公布AMG 191用于正在接受异基因造血细胞移植患者,治疗骨髓增生异常综合征和急性髓系白血病的1期试验JSP-CP-003(NCT04429191)数据。研究结果显示,6例在移植前接受单剂量AMG 191治疗的患者成功接受了造血细胞移植,第90天时,5例患者观察到完全的供体骨髓嵌合(≥95%),MRD呈阴性,另1例表现出MRD降低。AMG 191是一种FIC靶向CD117单抗,通过阻断干细胞因子受体信号传导,清除骨髓中的造血干细胞,为供体或基因矫正后的移植干细胞创造空间。
8.霍奇金淋巴瘤和非霍奇金淋巴瘤
2021-05-26:ADC公布了camidanlumab tesirine治疗霍奇金淋巴瘤和非霍奇金淋巴瘤的1期试验(NCT02432235)数据。在所有患者中,ORR达到58%,CR为29%。在霍奇金淋巴瘤亚组中,ORR为71%,CR为42%。其中2期研究推荐剂量(45 μg/kg)亚组的ORR达到86%,CR为49%。在非霍奇金淋巴瘤亚组中,ORR为38%,CR为9%。Camidanlumab tesirine是一种靶向CD25的ADC,偶联PBD二聚体。
9.实体瘤
2021-05-19:MacroGenics公布MGC018治疗晚期实体瘤的1期试验(NCT03729596)初步安全性和抗肿瘤活性数据。在剂量递增部分,mCRPC亚组中,5例患者(5/9)观察到PSA水平下降≥50%,8例患者观察到SD最佳响应;黑素瘤亚组中,3例患者最佳响应的目标病灶减少达到24%,28%和36%。在mCRPC剂量扩展部分,50%(11/22)患者PSA水平下降≥50%。MGC018是一种靶向B7-H3的ADC,偶联多卡霉素有效载荷,DAR约为2.7。
10.NRG1+实体瘤
2021-05-19:Merus公布zenocutuzumab治疗NRG1+实体瘤的1/2期试验eNRGY(NCT02912949)中期数据。研究结果显示,所有NRG1+实体瘤患者中,ORR达到27%(9/33);胰腺癌亚组中,ORR为40%(4/10)。Zenocutuzumab表现出良好的耐受性,常见的不良事件主要为轻度或中度。Zenocutuzumab是一种ADCC增强的,抑制NRG1+实体瘤中神经调节蛋白/HER3信号通路的,靶向HER2/HER3的双抗。
11.复发HPV相关癌症
2021-05-20:PDS Biotech公布了PDS0101治疗复发HPV相关癌症的2期试验(NCT04287868)中期数据。研究结果显示,ORR达到71%(10/14),1例肛门癌患者达到CR,9例达到PR(3例宫颈癌,2例阴道癌,2例肛门癌,2例口咽癌)。PDS0101是一种基于脂质体的HPV治疗性疫苗。PDS Biotech正在一项2期研究中评估PDS0101和帕博利珠单抗的组合,用于复发性或转移性头颈癌的一线治疗。
来源:NextPharma数据库
- 评论